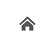細胞診標本作製工程
前処置
現在では、婦人科検体を主とした液状化細胞診(LBC)が普及してきている。これは、ブラシ等で採取した細胞を細胞保存液中に洗い落とし、フィルターで細胞を吸着し、乾燥しないうちにスライドグラスに吹き付け固定する方法である。
・ メリット
(1) 細胞が均等に塗布され顕微鏡下で見やすく、観察する範囲が一定であるため、見落としのリスクが軽減される。
(2) 保存液中の細胞は数週間安定で、同様の標本を複数枚作製可能で、免疫染色や遺伝子検査に対応できる。
・ デメリット
(1) 機器や消耗品が高価である。
(2) 処理法によっては溶血操作が必要である。

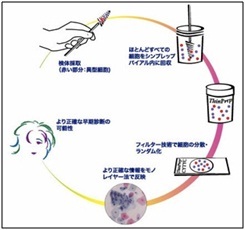
液状化細胞診(LBC)標本作成に於いては、現在では2つの方法に大別できます。一つは保存液中の細胞をフィルターで吸着しスライドガラス面に吹き付ける”ThinPrep法”と、採取細胞を分離剤にいれ比重勾配により細胞を採取する”シュアパス法”がある。写真はThinPrep法によるLBC標本作製機器である。内部に細胞保存液ボトルとスライドガラス、フィルターがセットされている。
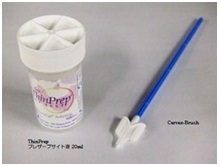 以前より子宮頚部からの細胞採取は綿棒で行われていたが、これからは写真のようなプラスチックブラシの使用が推奨されている。綿棒では細胞がトラップされるため塗抹が少数で、多くが廃棄されていましたが、ブラシを使用し写真の保存液中に洗い出す事によりそのほとんどが細胞診のみならず、HPVテスト等の検査に利用される事が可能となる。なお保存液での保存可能期間は6週間である。
以前より子宮頚部からの細胞採取は綿棒で行われていたが、これからは写真のようなプラスチックブラシの使用が推奨されている。綿棒では細胞がトラップされるため塗抹が少数で、多くが廃棄されていましたが、ブラシを使用し写真の保存液中に洗い出す事によりそのほとんどが細胞診のみならず、HPVテスト等の検査に利用される事が可能となる。なお保存液での保存可能期間は6週間である。
検体塗抹
・ 採取細胞をスライドグラスへの直接塗抹(直接塗抹法)
・ 遠心分離後、沈渣を擦り合わせ法もしくはストリッヒ法で塗抹
・ オートスメア法にて塗抹(細胞成分少数、検体量少量)
・ LBC材料の標本作製機器での塗抹(下記図)
1. ブラシで細胞を採取
2. 保存液中でブラシ洗浄
3. フィルター吸引後、スライドグラスへ吹き付け塗抹
4. 固定・染色・鏡検
固定操作 (30分以上)
・パパニコロウ染色の固定液は95%エタノール
・ギムザ染色の固定液はメタノールもしくはメイ・グリュンワルド液
注意点
・パパニコロウ染色用標本は乾燥厳禁(湿潤固定厳守/2秒以内)
・ギムザ染色用標本は塗布後速やかに冷風乾燥
染色
・パパニコロウ染色は染色性に透明感が有り、個々の細胞では核クロマチンや細胞質内の観察、細胞集塊の観察や組織型の判定に有効である
・ ギムザ染色標本は核。細胞質ともに乾燥肥大するためクロマチンや細胞質顆粒の観察や血液系細胞の判定に有効である
・パパニコロウ染色液及び含有色素
核染 : ヘマトキシリン
細胞質: OG6液(オレンジG)、EA50液(ビスマルクブラウン、エオジンY、ライトグリーンSF)
封入
・ キシレン透徹後、速やかに封入剤(ビオライト、エンテラン等)で封入する
・ 気泡の混入に注意
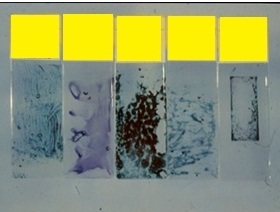
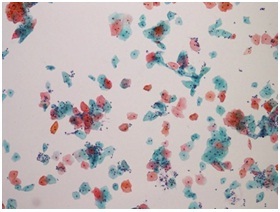
標本観察・診断
・ 細胞検査士の主要な業務は細胞診専門医へ提出し診断を受けるべき標本か否かを篩い分ける、所謂。スクリーニング検査である。
・ 細胞検査士は細胞診検査の最前線に位置し、個々の細胞を観察し判定するスペシャリストであり、異型細胞の見落としや標本の取り違い等は決して許されない。それゆえ、厳重な体調管理や 鏡検後の標本の再チェックなど、厳しい精度管理が行われている。

パパニコロウ染色(自動染色装置SAKURA DRS2000)
・ 染色時間は、
| 項目 | 通常法 | (お湯使用) | <術中迅速法> |
|---|---|---|---|
| (1) 95%アルコール | 1分 | (1分) | <11秒> |
| (2) 70%アルコール | 1分 | (1分) | <11秒> |
| (3) 50%アルコール | 1分 | (1分) | <11秒> |
| (4) 水洗 | 30秒 | (30秒) | <11秒> |
| (5) ギル・ヘマトキシリン | 3分 | (2分) | <30秒> |
| (6) 水洗 | 30秒 | (30秒) | <11秒> |
| (7) 0.5%塩酸アルコール | 90秒 | (1分) | <20秒> |
| (8) 水洗 | 15分 | (30秒) | <11秒> |
| (9) 温湯 | (1分) | <15秒> | |
| (10)水洗 | (30秒) | <11秒> | |
| (11)50%アルコール | 1分 | (1分) | <11秒> |
| (12)70%アルコール | 1分 | (1分) | <11秒> |
| (13)95%アルコール | 1分 | (1分) | <11秒> |
| (14)オレンジG | 2分 | (2分) | <48秒> |
| (15)95%アルコール | 30秒 | (30秒) | <11秒> |
| (16)EA50 (1) | 1分 | (1分) | <15秒> |
| (17)EA50 (2) | 1.5分 | (1.5分) | <20秒> |
| (18)100%アルコール (1) | 30秒 | (30秒) | <11秒> |
| (19)100%アルコール (2) | 1分 | (1分) | <11秒> |
| (20)100%アルコール (3) | 1分 | (1分) | <11秒> |
| (21)100%アルコール (4) | 2分 | (2分) | <11秒> |
| (22)100%アルコール (5) | 2分 | (2分) | <11秒> |
| (23)キシレン (1) | 30秒 | (30秒) | <11秒> |
| (24)キシレン (2) | 1分 | (1分) | <11秒> |
| (25)キシレン (3) | 1分 | (1分) | <11秒> |
| (26)キシレン (3) | 2分 | (2分) | <11秒> |
| (27)キシレン (5) | 終了 |
ギムザ染色
(1) メイグリュンワルド(MG)液 (MG液 15ml + メタノール 45ml) 5分
(2) ギムザ液(ギムザ液 5ml + 1/15 M リン酸緩衝液(ph 6.5)150ml) 60分
(3)水洗、乾燥、封入
検鏡・報告
1) 判定・ 判定はクラス分類を用いる。この分類はパパニコロウ分類を基に判定区分の 番号化をしたものである。
Class 1 : 異型または異常細胞を認めない
Class 2 : 良性と考えられる異型細胞を認める。中等度以上の炎症性変化がみられる
Class 3 : 悪性の疑いがある異型細胞を認めるが悪性といいきれない、前癌病変または境界悪性と考えられる(または疑う)異型細胞を認める
Class 4 : 悪性の疑いがある異型細胞を認める
Class 5 : 悪性と考えられる異型細胞を認める
・検体不適正の場合は「判定不能」とし、検体不適正の根拠を所見に明記する
・子宮頸部については日母分類に準拠して、Class3をaとbに分けてもかまわない
・三段階表記分類(陰性、疑陽性、陽性)に置き換えると、Class1, Class2は”陰性”、Class3は”疑陽性”、Class4, Class5は”陽性”と解されるものとする
・乳腺および甲状腺の細胞診報告様式に置き換えると、Class1, Class2は”正常あるいは良性”、Class3は”鑑別困難”、Class4は”悪性の疑い”、Class5は”悪性”と解されるものとする